ரேடியம்: திருத்தங்களுக்கு இடையிலான வேறுபாடு
சி r2.7.2+) (தானியங்கி இணைப்பு: br:Radiom |
|||
| (13 பயனர்களால் செய்யப்பட்ட 22 இடைப்பட்ட திருத்தங்கள் காட்டப்படவில்லை.) | |||
| வரிசை 1: | வரிசை 1: | ||
{{தகவற்சட்டம் ரேடியம்}} |
|||
'''கருகன் (ரேடியம்)''' என்பது ஒரு கதிர்வீச்சு இயல்புள்ள ஒரு [[தனிமம்|தனிமமாகும்]] (மூலகமாகும்). இதன் குறியீடு '''Ra'''. இதன் [[அணு எண்]] 88 ஆகும். இது பொதுவாக தூய வெள்ளை நிறமாக இருப்பினும் வளியில் திறந்துவிடப்படுபோது ஒட்சியேற்றப்பட்டு [[கறுப்பு]] நிறமாக மாறுகின்றது. இது கதிர்வீச்சை வெளியிடும் தன்மை கொண்டது. |
|||
'''ரேடியம்''' ''(Radium)'' என்பது Ra என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட கதிர்வீச்சு இயல்புள்ள ஒரு தனிமமாகும். இதன் அணு எண் 88 ஆகும். இதன் அணுநிறை 226 ஆகும். தனிம வரிசை அட்டவணையின் நெடுங்குழு 2 இல் இடம்பெற்றுள்ள ஆறாவது தனிமம் ரேடியம் ஆகும். காரமண் உலோகம் என்றும் இதை வகைப்படுத்துவர். தூய்மையான ரேடியம் வெள்ளியைப் போல வெண்மை நிறமுடையதாக உள்ளது. ஆனால் காற்றில் வெளிப்பட நேர்ந்தால் ரேடியம் ஆக்சிசனுக்குப் பதிலாக நைட்ரசனுடன் உடனடியாக வினைபுரிந்து ரேடியம் நைட்ரைடு (Ra3N2) என்ற கருப்பு நிற மேற்பரப்பு அடுக்காக உருவாகிறது. ரேடியத்தின் அனைத்து ஐசோடோப்புகளும் அதிகமான கதிரியக்கத் தன்மையுடையனவாகும். இவற்றில் ரேடியம் -226 என்ற ஐசோடோப்பு அதிக நிலைப்புத்தன்மை கொண்டதாக உள்ளது. இதனுடைய அரை ஆயுள் காலம் 1600 ஆண்டுகளாகும். கதிரியக்கச் சிதைவடைந்து இந்த ஐசோடோப்பு ரேடான் வாயுவாக, குறிப்பாக ரேடான் - 222 என்ற ஐசோடோப்பாக மாறுகிறது. ரேடியம் சிதைவடையும்போது அயனியாக்கும் கதிர் ஒரு விளைபொருளாகும். இது ஒளிரும் வேதிப்பொருட்களை கிளர்வூட்டி கதிரியக்க ஒளிர்வைத் தருகிறது. |
|||
== வெளி இணைப்புகள் == |
|||
{{Commons|Radium}} |
|||
ரேடியம் குளோரைடு வடிவத்தில் ரேடியம் 1898 ஆம் ஆண்டு மேரிகியூரி மற்றும் பியரிகியூரி தம்பதியரால் கண்டறியப்பட்டது. பிரஞ்சு அறிவியல் அகாதமியில் யுரேனைட்டு என்ற கனிமத்திலிருந்து ரேடியம் தனித்துப் பிரித்தெடுக்கப்பட்டு ஐந்து நாட்களுக்குப் பின்னர் வெளியிடப்பட்டது. மேரிகியூரியும் ஆன்றே -லூயிசு டெபியர்ன் ஆகியோர் 1911 ஆம் ஆண்டு ரேடியம் குளோரைடை மின்னாற்பகுப்பு செய்து ரேடியத்தை அதனுடைய உலோக நிலையில் தயாரித்தனர்<ref>{{Cite web|url=http://www.rsc.org/periodic-table/element/88/radium|title=Radium|publisher=Royal Society of Chemistry }}</ref> |
|||
* [http://www.webelements.com/webelements/elements/text/Ra/index.html WebElements.com - Radium] (also used as a reference) |
|||
* [http://www.lateralscience.co.uk/radium/RaDisc.html Lateral Science - Radium Discovery] |
|||
இயற்கையில் ரேடியம் யுரேனியம் மற்றும் தோரியம் தாதுக்களில் மிகச்சிறிய அளவில் காணப்படுகிறது. வாழும் உயிரினங்களுக்கு ரேடியம் ஒன்றும் அத்தியாவசியமான தேவையாக இல்லை. இதன் கதிரியக்க மற்றும் இரசாயன வினைத்திறன் காரணமாக உயிர் வேதியியல் செயல்முறைகளில் இணைந்திருக்கும்போது, ஆரோக்கியத்திற்கு பாதகமான விளைவுகள் ஏற்படலாம். அணுக்கரு மருத்துவத்தில் பயன்படுவதைத் தவிர்த்து ரேடியத்திற்கு என வேறு வணிகப்பயன்பாடுகள் ஏதுமில்லை. முன்னர் இது கதிர் ஒளி வீசுகின்ற சாதனங்களுக்கான கதிரியக்க ஆதாரமாக பயன்படுத்தப்பட்டது. மேலும் இது பிணி நீக்கும் மருந்தாக கருதப்பட்டு கதிரியக்க போலி மருத்துவத்திலும் பயன்படுத்தப்பட்டது. இன்று இத்தகைய பயன்பாடுகளுக்காக ரேடியம் பயன்படுத்தப்படுவதில்லை. ஏனெனில் ரேடியத்தின் நச்சுத்தன்மை இன்று உணரப்பட்டுவிட்டது. எனவே குறைந்த நச்சுத்தன்மை கொண்ட ஐசோடோப்புகள் இக்கருவிகளில் பயன்படுத்தப்படுகின்றன. |
|||
==பண்புகள் == |
|||
அறியப்பட்டுள்ள காரமண் உலோகங்களில் மிகவும் கனமான உலோகம் ரேடியம் ஆகும். மற்றும் அக்குழுவில் இடம்பெற்றுள்ள ஒரே கதிரியக்க உலோகமும் இதுவேயாகும். ரேடியத்தின் இயற்பியல் மற்றும் வேதியியல் பண்புகள் பேரியம் தனிமத்தின் பண்புகளை ஒத்ததாக உள்ளது. |
|||
தூய ரேடியம் ஓர் ஆவியாகக் கூடிய தனிமமாகும். இதன் இலேசான இணை தனிமங்களாகக் கருதப்படும் கால்சியம், இசுட்ரோன்சியம் மற்றும் பேரியம் ஆகியவை சிறிய மஞ்சள் நிறத்தில் இருந்தாலும் இது வெள்ளியைப் போல வெண்மை நிறத்துடன் காணப்படுகிறது. |
|||
இதனுடைய நிறம் காற்றில் விரைவாக மங்கிவிடுகிறது. காற்றுடன் வினைபுரிந்து ரேடியம் நைட்ரைடு கருப்பு படலமாக இதன் மேற்பரப்பில் உருவாகிறது. ரேடியத்தின் உருகு நிலை 700 பாகை செல்சியசு வெப்ப நிலை அல்லது 960 பாகை செல்சியசு வெப்பநிலை இவற்றில் ஒன்றாக இருக்கலாம். மற்றும் இதனுடைய கொதி நிலை 1737 பாகை செல்சியசு வெப்பநிலை ஆகும். இவ்விரு அளவுகளும் பேரியத்தைக் காட்டிலும் குறைவான அளவுகளாக உள்ளன. தனிமவரிசை அட்டவணையின் ஆவர்த்தன போக்குகளுக்கு உட்பட்டதாகவும் இந்த அளவுகள் உள்ளன<ref name="Lide2004">{{cite book|last = Lide|first=D. R. |title = CRC Handbook of Chemistry and Physics |url = https://archive.org/details/crchandbookofche81lide|edition = 84th |location = Boca Raton (FL) |publisher = CRC Press |date = 2004 |isbn = 978-0-8493-0484-2}}</ref> . அட்டவணையின் மேலிருந்து கீழாகச் செல்லும்போது நெடுங்குழு 2 இன் தனிமங்கள் இத்தகைய போக்கையே காட்டுகின்றன. பேரியம் மற்றும் கார உலோகங்களைப் போல ரேடியம் சாதாரண வெப்ப நிலை மற்றும் அழுத்தத்தில் பொருள் மைய கனசதுர வடிவில் படிகமாகிறது. ரேடியம்-ரேடியம் பிணைப்பின் பிணைப்பு இடைவெளி 514.8 பைக்கோ மீட்டர்களாகும். இதன் அடர்த்தி 5.5 கிராம்/செ.மீ3 ஆகும். இது பேரியத்தின் அடர்த்தியைக் காட்டிலும் அதிகமாகும். ரேடியம்-பேரியம் அடர்த்தி வீதம் ரேடியம்-பேரியம் அணு நிறை வீதத்துடன் ஒப்பிட்டு நோக்கத்தக்கதாக உள்ளது. ஏனெனில் இரண்டு தனிமங்களும் ஒரே மாதிரியான படிகக் கட்டமைப்பில் படிகமாகியுள்ளன. |
|||
== ஐசோடோப்புகள் == |
|||
நிறை எண்கள் 202 முதல் 234 வரை உள்ள 33 ஐசோடோப்புகளை ரேடியம் கொண்டுள்ளது. இவை அனைத்தும் கதிரியக்கச் செயல்பாடு கொண்டவையாகும். அரை ஆயுட்காலம் 11.4 நாட்களைக் கொண்ட 223Ra, அரை ஆயுட்காலம் 3.64 நாட்களைக் கொண்ட 224Ra , அரை ஆயுட்காலம் 1600 ஆண்டுகள் கொண்ட 226Ra, அரை ஆயுட்காலம் 5.75 ஆண்டுகள் கொண்ட 228Ra என்ற நான்கு ஐசோடோப்புகளும் தோரியம்-232, யுரேனியம்-235, மற்றும் யுரேனியம்-238 போன்ற ஐசோடோப்புகளின் சிதைவுச் சங்கிலியிலிருந்து இயற்கையாகத் தோன்றுகின்றன. 223Ra ஐசோடோப்பு யுரேனியம்-235 ஐசோடோப்பிலிருந்தும், 226Ra ஐசோடோப்பு யுரேனியம்-235 ஐசோடோப்பிலிருந்தும், மற்ற இரண்டு ஐசோடோப்புகளும் தோரியம் 232 ஐசோடோப்பிலிருந்தும் உருவாகின்றன. |
|||
== மேற்கோள்கள் == |
|||
{{Reflist}} |
|||
== வெளி இணைப்புகள் == |
|||
{{Commons|Radium|ரேடியம்}} |
|||
* [http://www.lateralscience.co.uk/radium/RaDisc.html Lateral Science – Radium Discovery] {{Webarchive|url=https://web.archive.org/web/20160309040715/http://lateralscience.blogspot.co.uk/2012/07/the-discovery-of-radium-by-marie-curie.html |date=2016-03-09 }} |
|||
* [http://www.markwshead.com/stuffHappens/radium.html Photos of Radium Water Bath in Oklahoma] |
* [http://www.markwshead.com/stuffHappens/radium.html Photos of Radium Water Bath in Oklahoma] |
||
* [http://toxnet.nlm.nih.gov/cgi-bin/sis/search/r?dbs+hsdb:@term+@na+@rel+radium,+radioactive NLM Hazardous Substances Databank – Radium, Radioactive] |
|||
* [http://www.lileks.com/institute/funny/07/40.html Reproduction of a 1942 comic book ad selling a "Radiumscope" to children] {{Webarchive|url=https://web.archive.org/web/20120427141925/http://www.lileks.com/institute/funny/07/40.html |date=2012-04-27 }} |
|||
* [http://alsos.wlu.edu/qsearch.aspx?browse=science/Radium Annotated bibliography for radium from the Alsos Digital Library for Nuclear Issues] {{Webarchive|url=https://web.archive.org/web/20190625210454/http://alsos.wlu.edu/qsearch.aspx?browse=science%2FRadium |date=2019-06-25 }} |
|||
* [http://www.japantoday.com/category/jt-experts/view/the-poisoner-next-door The Poisoner Next Door – Japan Today, 10/20/2001] |
|||
* [http://www.periodicvideos.com/videos/088.htm Radium] at ''The Periodic Table of Videos'' (University of Nottingham) |
|||
{{clear}} |
|||
{{ரேடியம் சேர்மங்கள்}} |
|||
{{stub}} |
|||
{{தனிம வரிசை அட்டவணை}} |
|||
{{Authority control}} |
|||
[[பகுப்பு:தனிமங்கள்]] |
[[பகுப்பு:தனிமங்கள்]] |
||
[[பகுப்பு:காரக்கனிம மாழைகள்]] |
[[பகுப்பு:காரக்கனிம மாழைகள்]] |
||
[[பகுப்பு:ரேடியம்| ]] |
|||
{{வார்ப்புரு:தனிம வரிசை அட்டவணை}} |
|||
[[als:Radium]] |
|||
[[am:ራዲየም]] |
|||
[[an:Radio (elemento)]] |
|||
[[ar:راديوم]] |
|||
[[arz:راديوم]] |
|||
[[az:Radium]] |
|||
[[be:Радый]] |
|||
[[be-x-old:Рад (элемэнт)]] |
|||
[[bg:Радий]] |
|||
[[bn:রেডিয়াম]] |
|||
[[br:Radiom]] |
|||
[[bs:Radij]] |
|||
[[ca:Radi (element)]] |
|||
[[co:Radiu]] |
|||
[[cs:Radium]] |
|||
[[cv:Ради]] |
|||
[[cy:Radiwm]] |
|||
[[da:Radium]] |
|||
[[de:Radium]] |
|||
[[el:Ράδιο]] |
|||
[[en:Radium]] |
|||
[[eo:Radiumo]] |
|||
[[es:Radio (elemento)]] |
|||
[[et:Raadium]] |
|||
[[eu:Radio]] |
|||
[[fa:رادیم]] |
|||
[[fi:Radium]] |
|||
[[fr:Radium]] |
|||
[[fur:Radi]] |
|||
[[ga:Raidiam]] |
|||
[[gl:Radio (elemento)]] |
|||
[[gv:Raadjum]] |
|||
[[hak:Luì]] |
|||
[[he:רדיום]] |
|||
[[hif:Radium]] |
|||
[[hr:Radij]] |
|||
[[ht:Radyòm]] |
|||
[[hu:Rádium]] |
|||
[[hy:Ռադիում]] |
|||
[[ia:Radium]] |
|||
[[id:Radium]] |
|||
[[io:Radiumo]] |
|||
[[is:Radín]] |
|||
[[it:Radio (elemento)]] |
|||
[[ja:ラジウム]] |
|||
[[jbo:dircyjinme]] |
|||
[[jv:Radium]] |
|||
[[kk:Радий]] |
|||
[[ko:라듐]] |
|||
[[ku:Radyûm]] |
|||
[[kv:Радий]] |
|||
[[la:Radium]] |
|||
[[lb:Radium]] |
|||
[[lij:Radio (elemento)]] |
|||
[[lt:Radis]] |
|||
[[lv:Rādijs]] |
|||
[[mi:Konuruke]] |
|||
[[mk:Радиум]] |
|||
[[ml:റേഡിയം]] |
|||
[[mr:रेडियम]] |
|||
[[mrj:Радий]] |
|||
[[ms:Radium]] |
|||
[[my:ရေဒီယမ်]] |
|||
[[nds:Radium]] |
|||
[[new:रेडियम]] |
|||
[[nl:Radium]] |
|||
[[nn:Radium]] |
|||
[[no:Radium]] |
|||
[[oc:Radi]] |
|||
[[pa:ਰੇਡੀਅਮ]] |
|||
[[pl:Rad (pierwiastek)]] |
|||
[[pnb:ریڈیم]] |
|||
[[pt:Rádio (elemento químico)]] |
|||
[[qu:Radyu q'illay]] |
|||
[[ro:Radiu]] |
|||
[[ru:Радий]] |
|||
[[sah:Радиум]] |
|||
[[scn:Ràdiu (elementu)]] |
|||
[[sh:Radijum]] |
|||
[[simple:Radium]] |
|||
[[sk:Rádium]] |
|||
[[sl:Radij]] |
|||
[[sr:Радијум]] |
|||
[[stq:Radium]] |
|||
[[sv:Radium]] |
|||
[[sw:Radi (elementi)]] |
|||
[[th:เรเดียม]] |
|||
[[tr:Radyum]] |
|||
[[ug:رادىي]] |
|||
[[uk:Радій]] |
|||
[[ur:ریڈیم]] |
|||
[[vep:Radii]] |
|||
[[vi:Radi]] |
|||
[[war:Radyo (elemento)]] |
|||
[[xal:Радиум]] |
|||
[[yi:ראדיום]] |
|||
[[yo:Radiomu]] |
|||
[[zh:镭]] |
|||
[[zh-classical:鐳]] |
|||
[[zh-yue:鐳]] |
|||
15:55, 13 மே 2024 இல் கடைசித் திருத்தம்
| ரேடியம் | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
88Ra
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| தோற்றம் | |||||||||||||||||||||||||||||||
வெள்ளி உலோக நிறம்
| |||||||||||||||||||||||||||||||
| பொதுப் பண்புகள் | |||||||||||||||||||||||||||||||
| பெயர், குறியீடு, எண் | ரேடியம், Ra, 88 | ||||||||||||||||||||||||||||||
| உச்சரிப்பு | /ˈreɪdiəm/ RAY-dee-əm | ||||||||||||||||||||||||||||||
| தனிம வகை | காரக்கனிம மாழைகள் | ||||||||||||||||||||||||||||||
| நெடுங்குழு, கிடை வரிசை, குழு | 2, 7, s | ||||||||||||||||||||||||||||||
| நியம அணு நிறை (அணுத்திணிவு) |
(226) | ||||||||||||||||||||||||||||||
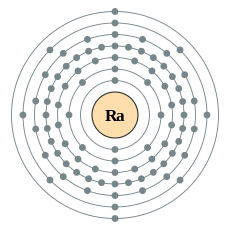
| இலத்திரன் அமைப்பு | [Rn] 7s2 2, 8, 18, 32, 18, 8, 2 | ||||||||||||||||||||||||||||||
| வரலாறு | |||||||||||||||||||||||||||||||
| கண்டுபிடிப்பு | பியேர் கியூரி மற்றும் மேரி கியூரி (1898) | ||||||||||||||||||||||||||||||
| முதற்தடவையாகத் தனிமைப்படுத்தியவர் |
மேரி கியூரி (1902) | ||||||||||||||||||||||||||||||
| இயற்பியற் பண்புகள் | |||||||||||||||||||||||||||||||
| நிலை | solid | ||||||||||||||||||||||||||||||
| அடர்த்தி (அ.வெ.நிக்கு அருகில்) | 5.5 g·cm−3 | ||||||||||||||||||||||||||||||
| உருகுநிலை | 973 K, 700 °C, 1292 °F | ||||||||||||||||||||||||||||||
| கொதிநிலை | 2010 K, 1737 °C, 3158.6 °F | ||||||||||||||||||||||||||||||
| உருகலின் வெப்ப ஆற்றல் | 8.5 கி.யூல்·மோல்−1 | ||||||||||||||||||||||||||||||
| வளிமமாக்கலின் வெப்ப ஆற்றல் | 113 கி.யூல்·மோல்−1 | ||||||||||||||||||||||||||||||
| ஆவி அழுத்தம் | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| அணுப் பண்புகள் | |||||||||||||||||||||||||||||||
| ஒக்சியேற்ற நிலைகள் | 2 (கார ஆக்சைடு) | ||||||||||||||||||||||||||||||
| மின்னெதிர்த்தன்மை | 0.9 (பாலிங் அளவையில்) | ||||||||||||||||||||||||||||||
| மின்மமாக்கும் ஆற்றல் | 1வது: 509.3 kJ·mol−1 | ||||||||||||||||||||||||||||||
| 2வது: 979.0 kJ·mol−1 | |||||||||||||||||||||||||||||||
| பங்கீட்டு ஆரை | 221±2 pm | ||||||||||||||||||||||||||||||
| வான்டர் வாலின் ஆரை | 283 பிமீ | ||||||||||||||||||||||||||||||
| பிற பண்புகள் | |||||||||||||||||||||||||||||||
| படிக அமைப்பு | body-centered cubic | ||||||||||||||||||||||||||||||
| காந்த சீரமைவு | nonmagnetic | ||||||||||||||||||||||||||||||
| மின்கடத்துதிறன் | (20 °C) 1 µΩ·m | ||||||||||||||||||||||||||||||
| வெப்ப கடத்துத் திறன் | 18.6 W·m−1·K−1 | ||||||||||||||||||||||||||||||
| CAS எண் | 7440-14-4 | ||||||||||||||||||||||||||||||
| மிக உறுதியான ஓரிடத்தான்கள் (சமதானிகள்) | |||||||||||||||||||||||||||||||
| முதன்மைக் கட்டுரை: ரேடியம் இன் ஓரிடத்தான் | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
ரேடியம் (Radium) என்பது Ra என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட கதிர்வீச்சு இயல்புள்ள ஒரு தனிமமாகும். இதன் அணு எண் 88 ஆகும். இதன் அணுநிறை 226 ஆகும். தனிம வரிசை அட்டவணையின் நெடுங்குழு 2 இல் இடம்பெற்றுள்ள ஆறாவது தனிமம் ரேடியம் ஆகும். காரமண் உலோகம் என்றும் இதை வகைப்படுத்துவர். தூய்மையான ரேடியம் வெள்ளியைப் போல வெண்மை நிறமுடையதாக உள்ளது. ஆனால் காற்றில் வெளிப்பட நேர்ந்தால் ரேடியம் ஆக்சிசனுக்குப் பதிலாக நைட்ரசனுடன் உடனடியாக வினைபுரிந்து ரேடியம் நைட்ரைடு (Ra3N2) என்ற கருப்பு நிற மேற்பரப்பு அடுக்காக உருவாகிறது. ரேடியத்தின் அனைத்து ஐசோடோப்புகளும் அதிகமான கதிரியக்கத் தன்மையுடையனவாகும். இவற்றில் ரேடியம் -226 என்ற ஐசோடோப்பு அதிக நிலைப்புத்தன்மை கொண்டதாக உள்ளது. இதனுடைய அரை ஆயுள் காலம் 1600 ஆண்டுகளாகும். கதிரியக்கச் சிதைவடைந்து இந்த ஐசோடோப்பு ரேடான் வாயுவாக, குறிப்பாக ரேடான் - 222 என்ற ஐசோடோப்பாக மாறுகிறது. ரேடியம் சிதைவடையும்போது அயனியாக்கும் கதிர் ஒரு விளைபொருளாகும். இது ஒளிரும் வேதிப்பொருட்களை கிளர்வூட்டி கதிரியக்க ஒளிர்வைத் தருகிறது.
ரேடியம் குளோரைடு வடிவத்தில் ரேடியம் 1898 ஆம் ஆண்டு மேரிகியூரி மற்றும் பியரிகியூரி தம்பதியரால் கண்டறியப்பட்டது. பிரஞ்சு அறிவியல் அகாதமியில் யுரேனைட்டு என்ற கனிமத்திலிருந்து ரேடியம் தனித்துப் பிரித்தெடுக்கப்பட்டு ஐந்து நாட்களுக்குப் பின்னர் வெளியிடப்பட்டது. மேரிகியூரியும் ஆன்றே -லூயிசு டெபியர்ன் ஆகியோர் 1911 ஆம் ஆண்டு ரேடியம் குளோரைடை மின்னாற்பகுப்பு செய்து ரேடியத்தை அதனுடைய உலோக நிலையில் தயாரித்தனர்[1]
இயற்கையில் ரேடியம் யுரேனியம் மற்றும் தோரியம் தாதுக்களில் மிகச்சிறிய அளவில் காணப்படுகிறது. வாழும் உயிரினங்களுக்கு ரேடியம் ஒன்றும் அத்தியாவசியமான தேவையாக இல்லை. இதன் கதிரியக்க மற்றும் இரசாயன வினைத்திறன் காரணமாக உயிர் வேதியியல் செயல்முறைகளில் இணைந்திருக்கும்போது, ஆரோக்கியத்திற்கு பாதகமான விளைவுகள் ஏற்படலாம். அணுக்கரு மருத்துவத்தில் பயன்படுவதைத் தவிர்த்து ரேடியத்திற்கு என வேறு வணிகப்பயன்பாடுகள் ஏதுமில்லை. முன்னர் இது கதிர் ஒளி வீசுகின்ற சாதனங்களுக்கான கதிரியக்க ஆதாரமாக பயன்படுத்தப்பட்டது. மேலும் இது பிணி நீக்கும் மருந்தாக கருதப்பட்டு கதிரியக்க போலி மருத்துவத்திலும் பயன்படுத்தப்பட்டது. இன்று இத்தகைய பயன்பாடுகளுக்காக ரேடியம் பயன்படுத்தப்படுவதில்லை. ஏனெனில் ரேடியத்தின் நச்சுத்தன்மை இன்று உணரப்பட்டுவிட்டது. எனவே குறைந்த நச்சுத்தன்மை கொண்ட ஐசோடோப்புகள் இக்கருவிகளில் பயன்படுத்தப்படுகின்றன.
பண்புகள்[தொகு]
அறியப்பட்டுள்ள காரமண் உலோகங்களில் மிகவும் கனமான உலோகம் ரேடியம் ஆகும். மற்றும் அக்குழுவில் இடம்பெற்றுள்ள ஒரே கதிரியக்க உலோகமும் இதுவேயாகும். ரேடியத்தின் இயற்பியல் மற்றும் வேதியியல் பண்புகள் பேரியம் தனிமத்தின் பண்புகளை ஒத்ததாக உள்ளது.
தூய ரேடியம் ஓர் ஆவியாகக் கூடிய தனிமமாகும். இதன் இலேசான இணை தனிமங்களாகக் கருதப்படும் கால்சியம், இசுட்ரோன்சியம் மற்றும் பேரியம் ஆகியவை சிறிய மஞ்சள் நிறத்தில் இருந்தாலும் இது வெள்ளியைப் போல வெண்மை நிறத்துடன் காணப்படுகிறது.
இதனுடைய நிறம் காற்றில் விரைவாக மங்கிவிடுகிறது. காற்றுடன் வினைபுரிந்து ரேடியம் நைட்ரைடு கருப்பு படலமாக இதன் மேற்பரப்பில் உருவாகிறது. ரேடியத்தின் உருகு நிலை 700 பாகை செல்சியசு வெப்ப நிலை அல்லது 960 பாகை செல்சியசு வெப்பநிலை இவற்றில் ஒன்றாக இருக்கலாம். மற்றும் இதனுடைய கொதி நிலை 1737 பாகை செல்சியசு வெப்பநிலை ஆகும். இவ்விரு அளவுகளும் பேரியத்தைக் காட்டிலும் குறைவான அளவுகளாக உள்ளன. தனிமவரிசை அட்டவணையின் ஆவர்த்தன போக்குகளுக்கு உட்பட்டதாகவும் இந்த அளவுகள் உள்ளன[2] . அட்டவணையின் மேலிருந்து கீழாகச் செல்லும்போது நெடுங்குழு 2 இன் தனிமங்கள் இத்தகைய போக்கையே காட்டுகின்றன. பேரியம் மற்றும் கார உலோகங்களைப் போல ரேடியம் சாதாரண வெப்ப நிலை மற்றும் அழுத்தத்தில் பொருள் மைய கனசதுர வடிவில் படிகமாகிறது. ரேடியம்-ரேடியம் பிணைப்பின் பிணைப்பு இடைவெளி 514.8 பைக்கோ மீட்டர்களாகும். இதன் அடர்த்தி 5.5 கிராம்/செ.மீ3 ஆகும். இது பேரியத்தின் அடர்த்தியைக் காட்டிலும் அதிகமாகும். ரேடியம்-பேரியம் அடர்த்தி வீதம் ரேடியம்-பேரியம் அணு நிறை வீதத்துடன் ஒப்பிட்டு நோக்கத்தக்கதாக உள்ளது. ஏனெனில் இரண்டு தனிமங்களும் ஒரே மாதிரியான படிகக் கட்டமைப்பில் படிகமாகியுள்ளன.
ஐசோடோப்புகள்[தொகு]
நிறை எண்கள் 202 முதல் 234 வரை உள்ள 33 ஐசோடோப்புகளை ரேடியம் கொண்டுள்ளது. இவை அனைத்தும் கதிரியக்கச் செயல்பாடு கொண்டவையாகும். அரை ஆயுட்காலம் 11.4 நாட்களைக் கொண்ட 223Ra, அரை ஆயுட்காலம் 3.64 நாட்களைக் கொண்ட 224Ra , அரை ஆயுட்காலம் 1600 ஆண்டுகள் கொண்ட 226Ra, அரை ஆயுட்காலம் 5.75 ஆண்டுகள் கொண்ட 228Ra என்ற நான்கு ஐசோடோப்புகளும் தோரியம்-232, யுரேனியம்-235, மற்றும் யுரேனியம்-238 போன்ற ஐசோடோப்புகளின் சிதைவுச் சங்கிலியிலிருந்து இயற்கையாகத் தோன்றுகின்றன. 223Ra ஐசோடோப்பு யுரேனியம்-235 ஐசோடோப்பிலிருந்தும், 226Ra ஐசோடோப்பு யுரேனியம்-235 ஐசோடோப்பிலிருந்தும், மற்ற இரண்டு ஐசோடோப்புகளும் தோரியம் 232 ஐசோடோப்பிலிருந்தும் உருவாகின்றன.
மேற்கோள்கள்[தொகு]
- ↑ "Radium". Royal Society of Chemistry.
- ↑ Lide, D. R. (2004). CRC Handbook of Chemistry and Physics (84th ed.). Boca Raton (FL): CRC Press. பன்னாட்டுத் தரப்புத்தக எண் 978-0-8493-0484-2.
வெளி இணைப்புகள்[தொகு]
- Lateral Science – Radium Discovery பரணிடப்பட்டது 2016-03-09 at the வந்தவழி இயந்திரம்
- Photos of Radium Water Bath in Oklahoma
- NLM Hazardous Substances Databank – Radium, Radioactive
- Reproduction of a 1942 comic book ad selling a "Radiumscope" to children பரணிடப்பட்டது 2012-04-27 at the வந்தவழி இயந்திரம்
- Annotated bibliography for radium from the Alsos Digital Library for Nuclear Issues பரணிடப்பட்டது 2019-06-25 at the வந்தவழி இயந்திரம்
- The Poisoner Next Door – Japan Today, 10/20/2001
- Radium at The Periodic Table of Videos (University of Nottingham)